异体移植突破跨物种器官移植壁 医学革命带来新希望
异体移植突破跨物种器官移植壁 医学革命带来新希望。深夜,某器官移植中心的重症监护室内,62岁的张建国注视着心电监护仪上跳动的曲线。这颗让他能够自主呼吸、正常交流的心脏并非人类心脏,而是一颗经过基因编辑的猪心。截至某个时间节点,这颗特殊的“生命引擎”已稳定工作200天,刷新了亚洲异种心脏移植的存活纪录,为无数徘徊在生死边缘的器官衰竭患者带来了希望。

中国每年约有30万器官衰竭患者,但仅有约2万人能获得移植机会,供需比例达到惊人的1:30。面对这一残酷现实,医学界将目光投向了一个看似疯狂却充满希望的方向——让猪的心脏、肾脏、肝脏在人体内“安家”。

2025年9月23日,西京医院完成了一例亚洲首例基因编辑猪-患者异种肾移植手术,移植猪肾已稳定工作超过200天,刷新亚洲纪录。这只被称为“内江猪”的基因编辑供体猪,在术后第6天即恢复了患者的血肌酐水平至正常范围,显示其代谢功能正常。此外,中科奥格与华中科技大学同济医院合作的猪-猴肾移植实验也取得重要进展,其中两例存活超过180天,最长一例已达330天,持续刷新亚洲非人灵长类异种移植存活纪录。
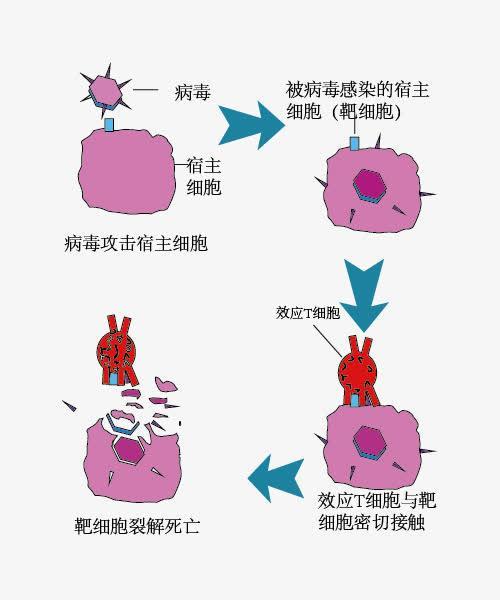
心脏移植领域同样捷报频传。张建国胸腔里那颗跳动了200天的基因编辑猪心脏不仅是时间的胜利,更是功能的证明。这头猪经过了多重基因改造,敲除了三个会引起人排斥反应的基因,并添加了多个人类转基因以提高兼容性。
肝移植也不甘示弱。2025年3月26日,中国空军军医大学西京医院的研究团队在《自然》杂志在线发表论文,报告了世界首例将基因编辑猪的肝脏移植到脑死亡人体内的成功案例。研究团队监测了10天内猪肝脏的功能、血流以及免疫和炎症反应,结果显示基因改造的猪肝脏能够在人体内存活并发挥功能,有望成为等待人类供体的肝衰竭患者的过渡疗法。
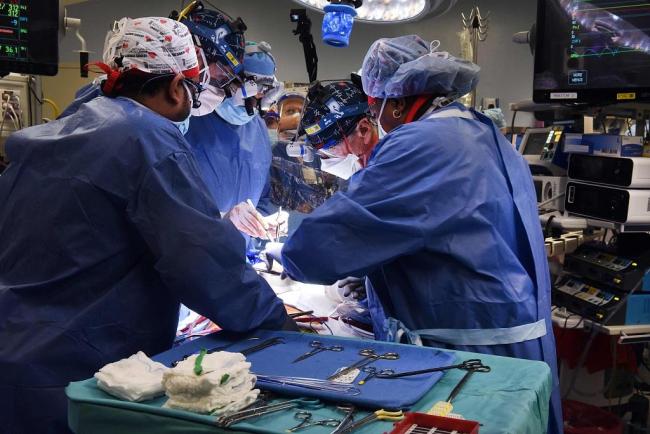
肺移植方面也有突破。某团队将经过六处基因编辑的巴马香猪左肺成功移植至39岁脑死亡患者体内。移植肺在216小时内保持通气功能,未出现超急性排斥或感染。这种“三删三加”策略使猪肺免疫原性降低83%,远超传统免疫抑制剂60%的抑制效果。
尽管临床突破不断,异种移植要真正走向成熟还需克服三大核心瓶颈。首先是超急性与慢性免疫排斥问题。科学家们通过敲除引发超急性免疫排斥的关键抗原α-Gal、Sda和Neu5Gc抗原,同时转入人源化补体调节蛋白及凝血调节蛋白等手段,成功降低了免疫排斥风险。然而,一旦发生排斥,逆转困难,可能导致严重后果。
其次是跨物种病毒传播的风险。猪内源性逆转录病毒(PERV)是一种潜在的跨物种传播风险。科研人员采用多重防线,包括人工筛选并排除携带病原体的猪、严格控制饮食以及使用CRISPR-Cas9等基因编辑手段灭活所有内源性逆转录病毒。
第三是伦理与监管问题。这类研究需遵循严格的伦理审查,涉及身份界定、宗教文化接受度、家属知情同意书等问题。此外,动物伦理也是一个棘手的问题,大规模繁殖、基因编辑并最终“收割”猪器官是否符合动物福利?
即便技术瓶颈逐一攻克,异种移植要真正惠及普通患者,还必须跨越产业化的鸿沟。首先是基因编辑猪的规模化与标准化,需要建立起从种猪筛选、基因编辑、无菌剖腹产到SPF饲养的完整产业链。其次是高昂的治疗成本,单例手术硬性投入超50万元,医保覆盖率不足40%。最后是长期安全性与有效性的时间检验,目前所有异种移植案例存活时间仍有限,缺乏十年、数十年的长期数据。
异种移植目前所处阶段是充满希望的突破性方向,但远非成熟、可大规模应用的即时解决方案。它是对抗器官短缺的重要战略路径之一,需与人体器官捐献、组织工程、人工器官等其他策略并行发展。或许在不久的将来,基因编辑猪器官将成为医院里的常规手术,但在那之前,我们还需要回答一个更深层的问题:当你的至亲躺在病床上等待一颗救命的心脏,而唯一的希望来自于一只经过基因编辑的猪时,你会做出怎样的选择?

